.
livello elementare
.
ARGOMENTO: EMERGENZA COVID
PERIODO: XXI SECOLO
AREA: PIANETA
parole chiave: Vaccini, CoVID 19
.
Abbiamo scoperto in un primo articolo i vaccini, come sono nati e quali siano i loro limiti. Ci eravamo lasciati sulla domanda forse più calda del momento: a quando i vaccini contro il CoVID 19?
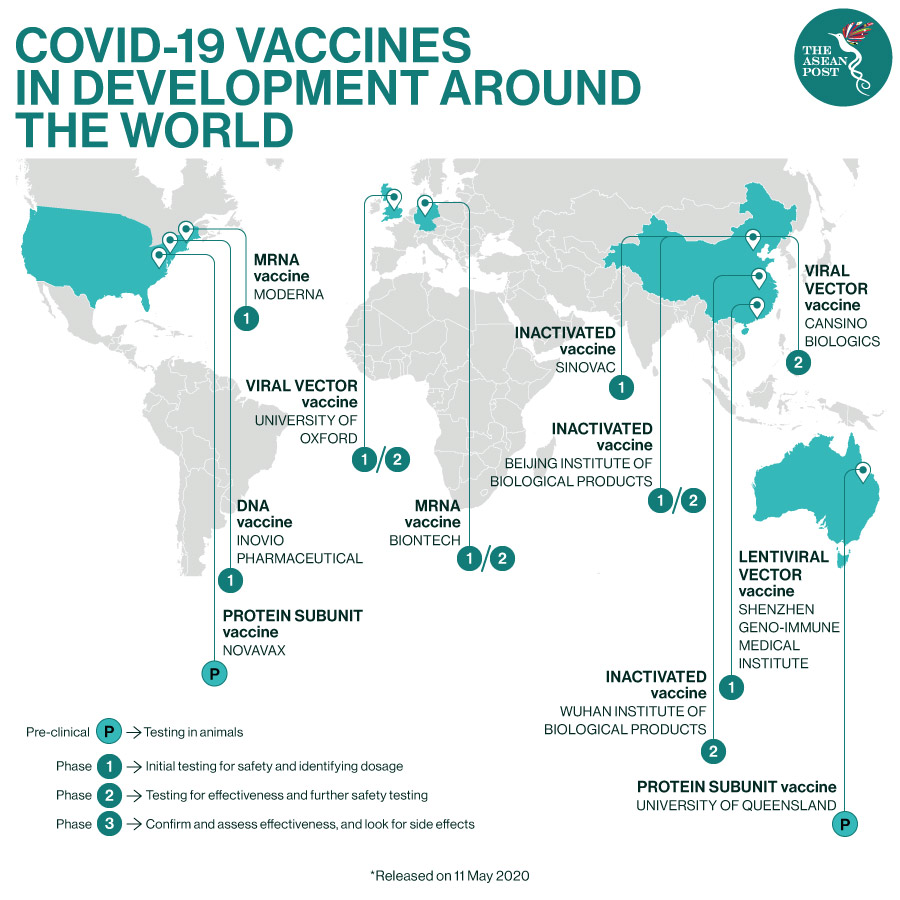
Sebbene la maggior parte degli oltre 200 candidati vaccini siano ancora coinvolti in fasi precliniche, sembrerebbe (il condizionale è d’obbligo) che una cinquantina abbiano raggiunto studi clinici avanzati e alcuni abbiano mostrato risultati promettenti.
Molte informazioni sono frammentarie per cui, conscio di non poter essere comunque esaustivo, ne elencherò lo stato dell’arte di alcuni tra i più citati sui media:
UNIVERSITÀ DI OXFORD / IRBM POMEZIA
Il vaccino ChAdOx1 nCoV-19 o AZD1222, più noto come vaccino Oxford, è stato realizzato dai ricercatori dell’Università di Oxford e dell’IRBM di Pomezia e sarà prodotto dall’azienda ASTRAZENECA. Il vaccino è stato giudicato efficace al 70% nella prevenzione del COVID-19 ma può arrivare al 90% se somministrato inizialmente con una mezza dose e, dopo un mese, con una dose intera. Il vaccino viene somministrato in due dosi, a 28 giorni di distanza l’una dall’altra ed è ancora in corso testato in studi clinici di fase 3 in tutto il mondo, inclusi Stati Uniti, Regno Unito e Brasile. Il vaccino è costituito da una versione indebolita di un comune virus del raffreddore, chiamato adenovirus. In pratica i ricercatori hanno alterato geneticamente il virus in modo che non potesse replicarsi negli esseri umani ed hanno aggiunto geni per codificare le cosiddette proteine spike che il coronavirus utilizza per infettare le cellule umane. Sembrerebbe che il vaccino abbia dimostrato di essere in grado di stimolare il sistema immunitario a produrre cellule T specifiche per SARS-CoV-2 – un gruppo di globuli bianchi importanti nella lotta contro i patogeni – e molecole che possono attaccarsi al virus e impedirgli di infettare le cellule. Una notizia dell’ultima ora afferma che scienziati britannici e russi stanno verificando se la combinazione di due vaccini contro il coronavirus (Oxford / AstraZeneca e Sputnik V) potrebbe portare a una protezione migliore rispetto a due dosi dello stesso. Non si hanno notizie certe sulla sua disponibilità per la vaccinazione.
CENTRO DI RICERCA GAMALEYA (SPUTNIK V)
Il Gamaleya Research Institute del Ministero della Salute russo ha sviluppato un vaccino contro il coronavirus, noto come “Sputnik V“, basato su due diversi virus del raffreddore. Questi virus sono geneticamente modificati per non replicarsi nell’Uomo e per codificare la proteina spike del coronavirus. La Russia ha annunciato il 24 novembre che il suo vaccino era efficace per oltre il 91,4% nella prevenzione del COVID-19, secondo i risultati di una seconda analisi del suo studio di fase 3. Ad agosto, il presidente Vladimir Putin ha annunciato che la Russia ha approvato il vaccino per l’uso su decine di migliaia di persone, prima che fosse accuratamente testato in studi clinici in fase avanzata. Ciò ha attirato numerose critiche internazionali. In realtà, secondo Science Magazine, il certificato di registrazione rilasciato dal Ministero della Salute russo ne ha approvato l’uso solo per un limitato gruppo di persone, compresi gli operatori sanitari. A settembre, i ricercatori hanno pubblicato i risultati dell fase 1 / fase 2 sulla rivista The Lancet. L’analisi, basata su 76 partecipanti ha suggerito che il loro vaccino era “sicuro e ben tollerato”.
SINOVAC BIOTECH
La società cinese, Sinovac Biotech, ha sviluppato e sta testando un vaccino chiamato CoronaVac, che è costituito da una versione inattivata del virus SARS-CoV-2. Secondo STAT News, la Sinovac Biotech ha in precedenza utilizzato la stessa tecnologia per sviluppare vaccini approvati per l’epatite A, l’epatite B, l’influenza suina, l’influenza aviaria e dell’afta epizootica. Il Coronavac, somministrato in due dosi a 14 giorni di distanza, sembra sia stato ben tollerato e abbia indotto una risposta immunitaria nei partecipanti, ma il numero di anticorpi prodotti è risultato inferiore a quelli ritrovati nei pazienti che avevano superato il COVID-19. La Cina ha approvato questo vaccino per uso di emergenza. Secondo Reuters (6 settembre) circa il 90% dei dipendenti di Sinovac e delle loro famiglie hanno assunto il vaccino sperimentale nell’ambito del programma di emergenza cinese. Sembra che il vaccino abbia concluso in novembre (TBC) una fase di sperimentazione 3 in Brasile con successo.
SINOPHARM
Il vaccino candidato del China National Pharmaceutical Group (Sinopharm) si basa su una forma inattivata di SARS-CoV-2. La società ha già iniziato la sperimentazione di fase 3 ad Abu Dhabi che, secondo Reuters, recluterà fino a 15.000 persone. Sempre secondo Reuters, la società ha anche avviato delle sperimentazioni di fase 3 in Perù e Marocco. Sinopharm sta testando anche un secondo vaccino sviluppato dal Beijing Institute of Biological Products in uno studio di fase 3 negli Emirati Arabi Uniti e in Argentina. Secondo la CNN, quasi un milione di persone ha già ricevuto il vaccino in Cina nell’ambito di un programma di emergenza.
MODERNA/U.S. National Institute of Allergy and Infectious Diseases (NIAID)
Questo candidato vaccino (mRNA-1273) è stato sviluppato dalla società biotecnologica americana Moderna e dal NIAID, ed è stato il primo ad essere testato sugli esseri umani negli Stati Uniti. MODERNA, il 16 di novembre, ha dichiarato che dall’analisi dei primi dati il vaccino è risultato efficace al 94,5% dei … 95 partecipanti alla fase tre. Il vaccino si basa su una tecnologia mai utilizzata fino ad ora, usando una parte di materiale genetico, ovvero l’RNA messaggero (mRNA), ritenendo che l’utilizzo del mRNA consenta una maggiore velocità e facilità per la produzione dell vaccino rispetto a quelli tradizionali. Sebbene i vaccini a mRNA potrebbero essere più durevoli contro patogeni che tendono a mutare, come i coronavirus e i virus influenzali, d’altro canto possono causare reazioni avverse nel corpo e hanno problemi di stabilità, cosa che, secondo National Geographic, potrebbe limitare la forza dell’immunità. La sperimentazione di fase 3 del vaccino di Moderna ha raggiunto i 30000 volontari con una validità del 94,1% e la Federal Drug Administration dovrebbe concedere entro il 21 dicembre l’autorizzazione all’uso del vaccino. Moderna prevede di produrre da 500 milioni a 1 miliardo di dosi a livello globale nel 2021.
PFIZER / BIONTECH
Pfizer e l’azienda biotecnologica tedesca BioNTech hanno, come Moderna, sviluppato un vaccino che utilizza l’RNA messaggero per spingere il sistema immunitario a riconoscere il coronavirus. I risultati contenuti in una prima analisi della fase 3, presentata il 18 novembre 2020, ha rivelato che il vaccino sia efficace al 95%. L’intenzione di Pfizer e BioNTech è di produrre fino a 50 milioni di dosi del suo vaccino a livello globale nel 2020 e fino a 1,3 miliardi di dosi del suo vaccino entro la fine del 2021. La sperimentazione di fase 3 continuerà comunque per altri due anni per raccogliere dati sulla sua sicurezza e efficacia. Il vaccino di Pfizer dovrebbe essere anch’esso somministrato in due dosi (come quello della Moderna) ma deve però essere conservato a temperature di meno 70 gradi C° (Moderna a meno 20 C°). La Food and Drug Administration statunitense ha sostenuto la proposta di autorizzare la distribuzione del vaccino anti-coronavirus in emergenza negli USA ed è stato approvato per la distribuzione di emergenza. Le vaccinazioni negli Stati Uniti sono iniziate il 14 dicembre. Italia e Germania stanno facendo pressione sull’Agenzia Europea del Farmaco per avere il beneplacito per iniziare al più presto le vaccinazioni.
AZIENDE FARMACEUTICHE JOHNSON & JOHNSON’S JANSSEN
Anche il vaccino sperimentale COVID-19 Janssen di Johnson & Johnson è basato su un adenovirus indebolito (ad26) e viene somministrato ai volontari come dose singola. Il vaccino utilizza un virus indebolito per fornire “informazioni” sul patogeno per stimolare la risposta immunitaria. Proprio come con altri vaccini COVID-19 basati su adenovirus, l’adenovirus indebolito esprime la proteina spike SARS-CoV-2. In particolare, Janssen sta usando la stessa tecnologia usata per sviluppare il suo vaccino contro l’Ebola. Johnson & Johnson ha iniziato gli studi di fase 3 negli Stati Uniti il 23 settembre. Il 15 novembre, Johnson & Johnson ha annunciato l’inizio di una nuova sperimentazione globale di fase 3 che studierà la sicurezza e l’efficacia di due dosi del vaccino (anziché una). Il vaccino Janssen di Johnson & Johnson sarà ora sottoposto all’esame finale della Food and Drug Administration per condurre la sperimentazione clinica del vaccino COVID-19 nelle Filippine.
NOVAVAX
La società statunitense Novavax sta testando un suo vaccino chiamato NVX-CoV2373. Secondo il New York Times, il vaccino, descritto come “vaccino con nanoparticelle ricombinanti“, è costituito da diverse proteine spike SARS-CoV-2 che vengono combinate in una nanoparticella insieme ad un adiuvante per il potenziamento immunitario. Il 2 settembre, i primi risultati degli studi di fase 1 / fase 2 sono stati pubblicati sul New England Journal of Medicine. Ai partecipanti sono state somministrate due dosi del vaccino a 21 giorni di distanza. Trentacinque giorni dopo la dose iniziale, i volontari hanno avuto risposte immunitarie superiori a quelle dei pazienti che hanno superato il COVID-19. Secondo la CNN, tutti i partecipanti hanno sviluppato anticorpi a livelli da quattro a sei volte superiori alla media di quelli sviluppati dai pazienti guariti. L’azienda ha anche avviato uno studio di fase 2 separato in Sud Africa, testando il loro candidato vaccino COVID-19 su volontari HIV-negativi e HIV-positivi. Il 24 settembre, Novavax ha annunciato di aver avviato la fase 3 dei test del vaccino nel Regno Unito con 10.000 volontari. NVX-CoV2373 è attualmente in uno studio di fase 3 nel Regno Unito e uno studio di fase 2b in Sud Africa, entrambi completamente avviati. Sebbene la Fase 3 per Stati Uniti e Messico sia stata ritardata, dovrebbe iniziare nelle prossime settimane.
Conclusioni
Questo stato dell’arte, è aggiornato al 15 di dicembre e le cose … corrono, forse anche troppo, cosa che fa intravedere una corsa politica senza precedenti al loro impiego. Certo tutti aspettiamo un vaccino che ci aiuti a mitigare il rischio del contagio ma va compreso che la certezza della sua efficacia non ci sarà fino a quando non si sarà generata una stabile immunità di gregge. Inoltre, i vaccini prescelti potranno essere distribuiti, se non in emergenza, solo quando la comunità scientifica avrà accertato in maniera assoluta la loro effettiva efficacia e sicurezza in base ai risultati sui volontari durante la fase 3. Partendo dal presupposto che comunque i vaccini non proteggono mai al 100%, non è però nemmeno sicuro per quanto tempo la protezione acquisita sarà effettivamente garantita.
Quale vaccino sarà prescelto in Italia?
Secondo Guido Rasi, direttore esecutivo dell’EMA, l’agenzia europea del farmaco, i vaccini russi e cinesi dovranno essere approvati dall’EMA prima della commercializzazione per cui ci vorrà molto tempo. Il ministro Speranza, pensa di avviare la vaccinazione anti Covid di 1,7 milioni di italiani già a partire dalla seconda metà di gennaio 2021 ed il candidato più probabile sembra essere il vaccino Pfizer-BionTech, appena autorizzato negli USA alla somministrazione. L’Agenzia Europea del Farmaco prenderà la sua decisione entro il 29 dicembre (anche se Italia e Germania stanno spingendo per avere l’autorizzazione il 21 dicembre). Intanto la Commissione Europea ha già negoziato un accordo di preacquisto per 200 milioni di dosi, estendibili a 300, da dividere fra i Paesi in base alla popolazione. Sembrerebbe che il ministro Speranza si sia accordato con la Pfizer per pianificare tempistica, dettagli tecnici e logistici per avviare la vaccinazione anti Covid di 1,7 milioni di italiani già a partire dalla seconda metà di gennaio 2021. Le notizie cambiano continuamente e per ora possiamo solo mantenere un comportamento prudente, per evitare la diffusione della pandemia.
In anteprima biochimici e virologi di tutto il mondo stanno conducendo ricerche utilizzando la tecnologia basata su CRISPR per ingegnerizzare geneticamente una contromisura antivirale dispiegabile per COVID-19. Il loro obiettivo è creare un antivirale personalizzabile per rispondere a molti virus diversi, incluso il coronavirus – Fonte U.S. Department of Energy United States COVID-19- DOE Response 507 001 008 (50039906843).jpg – Wikimedia Commons
Alcune delle immagini possono essere state prese dal web, citandone ove possibile gli autori e/o le fonti. Se qualcuno desiderasse specificarne l’autore o rimuoverle, può scrivere a infoocean4future@gmail.com e provvederemo immediatamente alla correzione dell’articolo